神外所刘福生团队《Advanced Functional Materials》阐述一种新型杂合纳米基因载体可提高脑胶质瘤化疗疗效
2019年3月,北京市神经外科研究所、附属北京天坛医院刘福生教授团队与北京化工大学徐福建教授团队在《Advanced Functional Materials》(IF:13.274)发表题为"A Hybrid Nanovector of Suicide Gene Engineered Lentivirus Coated with Bioreducible Polyaminoglycosides for Enhancing Therapeutic Efficacy against Glioma "的论文。研究团队构建了一种新型杂合纳米基因载体,体内外研究发现,该载体可通过增强CD(Cytosine Deaminase,胞嘧啶脱氨酶)自杀基因在胶质瘤细胞内的表达,进而提高无毒前体药物5-FC(5-fluorocytosine,5-氟胞嘧啶)治疗胶质瘤的疗效。北京市神经外科研究所、附属北京天坛医院范文华博士与北京化工大学邵玫瑜硕士为共同第一作者,刘福生教授与北京化工大学徐福建教授为共同通讯作者。

众所周知,胶质瘤是成人最常见的颅内肿瘤,患者确诊后尽管给予手术切除,并联合术后标准同步放化疗,但其预后存活率仍未超过14-20个月。基因治疗的出现被认为在癌症治疗中具有良好的应用前景,经过数十年研究探索,已经取得很大进展,为恶性胶质瘤的治疗带来新的曙光。但是如何构建既具有良好生物相容性又能实现高效基因转染效率的基因载体,成为基因治疗在临床中成功应用的瓶颈。
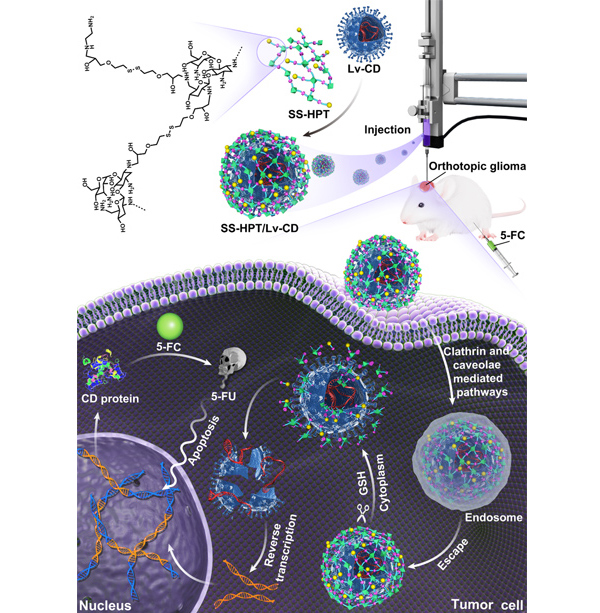
刘福生教授团队与徐福建教授团队,通过开展“医工”交叉合作,针对这一问题展开了探索性研究。在前期已成功合成“富羟基超支化氨基糖甙类阳离子聚合物(SS-HPT)”的基础上,该合作团队将此聚合物与自杀基因工程化的“慢病毒载体(Lv-CD)”通过静电相互作用,在体外进行自组装设计,构建了一种新型“杂合纳米基因载体(SS-HPT/Lv-CD nanohybrid)”,该载体直径约300nm,表面携带正电荷。在体外实验中,研究团队发现该载体并不是通过配体-受体结合的方式,而是通过静电相互作用结合的方式,使更多载体进入胶质瘤细胞内,并在细胞内高浓度的谷胱甘肽作用下,被快速降解,进而将自杀基因稳定整合在靶细胞基因组中。进一步研究发现,该载体不仅具有良好的血液相容性,而且不受血清等生物大分子的影响,并能显著提高慢病毒转染效率。在动物实验中,研究团队将该载体介导的自杀基因-前药治疗系统(CD/5-FC)用于胶质瘤的皮下及颅内模型中,发现与单纯慢病毒载体相比,该载体增强了自杀基因蛋白表达水平,并提高了前药5-FC对胶质瘤的疗效,延长实验动物的生存期。
该研究通过“医工”交叉合作,构建了一种新型杂合纳米基因载体,并发现其能提高胶质瘤的化疗疗效,为研发新型基因治疗载体提供了一种新的策略,也展现了基因治疗在胶质瘤等实体瘤中未来的应用价值,为临床上开展基因治疗提供了科学依据。

刘福生,教授,主任医师,研究员,博士研究生导师。首都医科大学附属北京天坛医院神经外科主任医师,北京市神经外科研究所脑肿瘤研究中心主任。北京市卫生系统高层次技术人才—神经外科学科带头人。主要从事颅内各种肿瘤的治疗,擅长岛叶及丘脑等复杂脑胶质瘤手术及颅内立体定向活检术。在科研方面,主要开展新型三维脑胶质瘤基因芯片的开发等转化医学研究,脑胶质瘤的生物学特性及溶瘤病毒-基因治疗脑胶质瘤的研究,以及病毒-基因治疗胶质瘤的新策略研究。共发表论文150余篇,其中SCI论文50余篇;获授权发明专利2项;主编《脑胶质瘤》和《脑胶质瘤基础与临床研究》;承担多项省部级以上课题,获国家科技进步二等奖、山东省科技进步一等奖、中华医学科技奖三等奖等。
