孙志伟教授团队AUTOPHAGY发文揭示纳米二氧化硅诱导自噬功能紊乱分子机制
2018年7月,我校公共卫生学院孙志伟教授团队牵头在AUTOPHAGY(IF:11.815)上发表论文,题目为"Silica nanoparticles induce autophagosome accumulation via activation of the EIF2AK3 and ATF6 UPR pathways in hepatocytes",该项研究阐述了纳米二氧化硅(SiO2)通过诱发内网应激并激活下游EIF2AK3(PERK)和ATF6信号通路从而诱导肝细胞自噬功能紊乱的分子机制。公共卫生学院王继副教授为第一作者,孙志伟教授与北京协和医学院赵振东教授为共同通讯作者。

纳米SiO2是一种产量较大的工程化纳米材料,被广泛应用于食品、化妆品、材料、化工和生物医药等领域。此外,纳米SiO2也是大气颗粒物(PM)的主要无机成分。随着工程化纳米SiO2应用范围的扩大和日益加重的大气污染问题,人群通过职业暴露、医源性暴露以及环境暴露途径接触纳米SiO2的机会不断增加,纳米SiO2已被国际经济合作与发展组织(OECD)列入需优先进行毒性评价的纳米材料。然而,目前缺乏标准化的纳米材料安全性评价体系,纳米SiO2对机体的有害效应尚未完全明确。因此,为确定纳米SiO2的潜在风险,有必要研究其生物学效应和毒理机制。
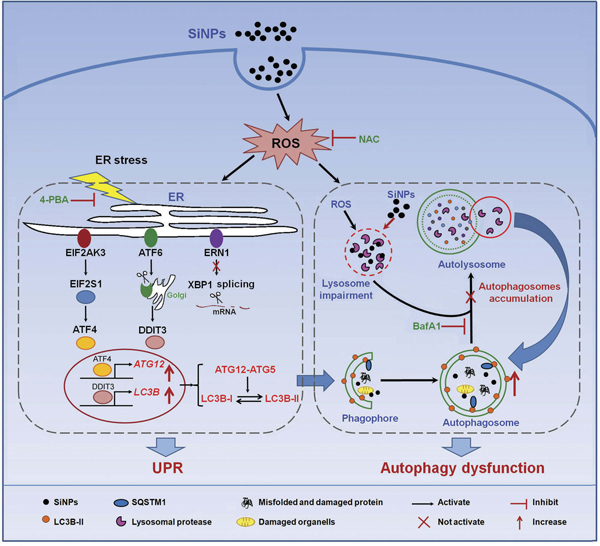
自噬功能紊乱是纳米材料的重要毒性机制之一。孙志伟教授团队长期致力于纳米SiO2毒性机制及安全性评价的研究,前期工作已证实纳米SiO2可引起肝毒性,并在肝细胞中研究发现纳米SiO2通过损伤溶酶体功能阻断自噬流抑制自噬体降解,诱导自噬功能紊乱。基于此,该研究从自噬体合成的角度深入探讨了纳米SiO2对自噬体形成的影响,结果表明纳米SiO2通过ROS诱发内质网应激,激活EIF2AK3(PERK)和ATF6信号通路,上调下游转录因子ATF4和DDIT3(CHOP),从而促进自噬基因ATG12和LC3B转录,增强自噬体合成,进而加剧自噬体积累,引起自噬功能紊乱,对细胞产生毒性。该研究为纳米SiO2的毒性机制和安全性评价研究提供了新的理论依据。
该研究课题由国家自然科学基金项目资助。
